证券代码:300204
证券简称:舒泰神
公告编号:2019-49-01
舒泰神(北京)生物制药股份有限公司
舒泰神(北京)生物制药股份有限公司
关于STSG-0002注射液获得新药临床试验通知书的公告
1、药品名称:STSG-0002注射液
2、通知书号:CXSL1900065
3、申请人:北京三诺佳邑生物技术有限责任公司、舒泰神(北京)生物制药股份有限公司
4、审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,2019年06月27日受理的STSG-0002注射液符合药品注册的有关要求,同意按照提交的方案开展慢性乙型肝炎的临床试验。
二、药品其他相关情况
STSG-0002注射液是具有自主知识产权的国家I类治疗用生物制品,公司及子公司三诺佳邑于2019年06月18日向国家药品监督管理局申报关于STSG-0002注射液的新药临床试验申请并于2019年06月27日获得受理,属于“特殊审批程序”品种。
STSG-0002注射液本次申报临床试验的适应症为:慢性乙型肝炎。乙型肝炎病毒(HBV)感染是严重威胁全球健康的主要问题之一。根据WHO发布的《Global hepatitis report, 2017》,全球有超过2.57亿人慢性感染;每年有超过88.7万人死于该病毒。中国是HBV高发国家,2006年中国HBV血清流行率调查显示,中国1~59岁人群的HBsAg携带率为7.18 %。因此,估计中国约有9300万人感染了乙肝病毒,其中2000万为乙肝病毒慢性乙肝患者。慢性乙型肝炎给患者的生活带来巨大的痛苦和经济负担。
目前在中国已上市的抗HBV核苷(酸)类(nucleos(t)ide, NAs)药物包括核苷类的拉米夫定(Lamivudine,LAM)、替比夫定(Telbivudine, LDT)、恩替卡韦(Entecavir,ETV)和核苷酸类的阿德福韦(Adefovir, ADV)、替诺福韦(Tenfovir,TDF)。NA类药物可通过抑制DNA逆转录酶活性而抑制HBV的复制,尽管现有的抗病毒治疗药物能够有效降低患者血清中HBV DNA的拷贝数,甚至达到检测下线水平,但是这些药物对HBsAg(乙型肝炎表面抗原)和HBeAg(乙型肝炎E抗原)的产生无直接抑制作用。目前国际慢性乙型肝炎的治疗方法均无法有效降低HBsAg抗原,其是导致肝硬化、肝癌的促进因素。此外,干扰素(interferon IFN)具有直接抗病毒作用和免疫调节作用,可有效提高机体免疫力,但只能注射给药,持续应答率低,副作用多且治疗费用高昂。
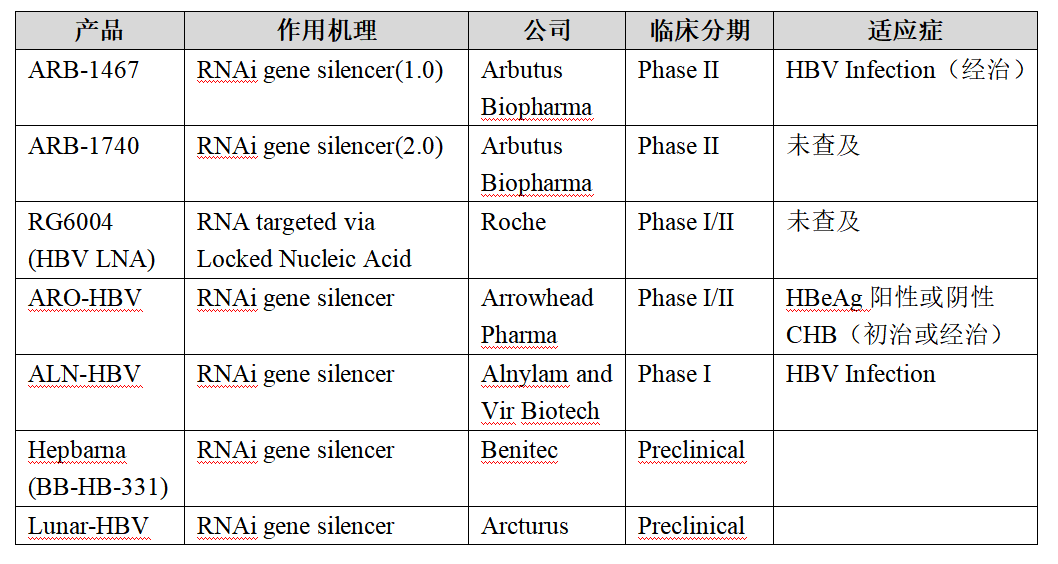
目前致力于HBV小干扰RNA作用机制的研发产品共有6家公司的7个产品,5个产品均处于临床I期和II期。根据临床试验注册情况,均以HBeAg阳性或阴性慢性乙型肝炎作为首选适应症进行开发,具体见下表:
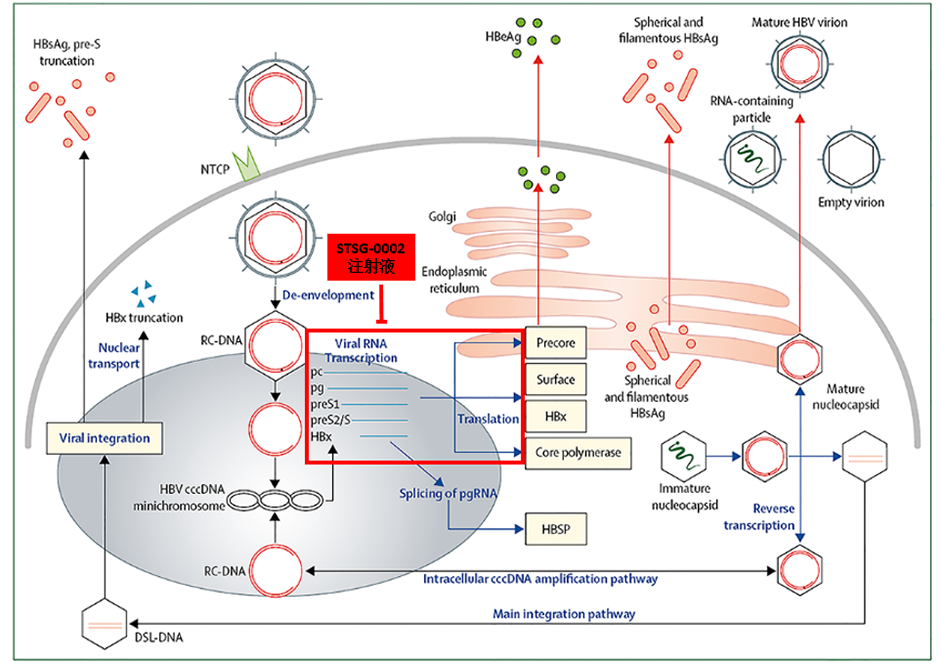
从作用机制上,STSG-0002注射液为携带靶向HBV基因组P区和X区的shRNA序列表达框的肝噬性复制缺陷重组腺相关病毒。它以重组腺相关病毒(rAAV)作为递送载体,将目的基因序列导入细胞转录生成shRNA,shRNA在细胞质中剪切为单链siRNA,随后通过RNAi机制,特异性地沉默HBV复制相关的pgRNA和HBV蛋白表达相关的sRNA,阻断HBV病毒复制,降低HBsAg、HBeAg和HBc蛋白的合成和分泌。STSG-0002具有明显嗜肝性,单次静脉给药可在肝细胞内长期表达siRNA。HBsAg的大幅度降低有望促进HBsAg血清转化,从而实现HBV功能性治愈。其作用机制示意图如下:
STSG-0002采用了重组腺相关病毒(rAAV)作为递送载体,由于其具有安全性好、特异性强、递送效率高、长期有效等特点,这一类递送系统已经被广泛应用于基因治疗领域,截止2018年底,已经有145项以AAV作为递送载体的临床研究在全球开展。
基因治疗药物的生产工艺较其他生物制品更为复杂,质量研究难度大,具有较高的技术门槛。公司经过多年持续投入和积累,形成了完善的基因治疗药物研究开发体系。在此基础上开发的STSG-0002注射液在递送效率、生产制备工艺、质量控制等多方面均达到了同类产品的世界领先水平,具有极强的技术竞争力。
在采用HBV转基因小鼠模型进行的临床前有效性研究中,STSG-0002注射液表现出卓越的有效性和长效性,特别是在降低HBV相关抗原方面较已有的NAs类药物恩替卡韦表现出明显优势。该研究采用NAs类药物恩替卡韦每日给药一次的作为对照组,而STSG-0002注射液在整个研究中只给药一次,实验观察检测周期总共长达9个月。研究发现:
1)STSG-0002注射液在给药后的第一个检测时间点(给药后7天)即表现出对血清中HBV DNA滴度的明显抑制效果,该抑制效果在整个实验观察期中保持稳定,直到最后一个检测时间点(给药后252天)未见HBV DNA滴度反弹。
2)值得关注的是,在针对HBsAg和HBeAg的检测中STSG-0002较恩替卡韦表现出明显的优势。恩替卡韦给药组未表现出与空白对照组在血清中HBsAg和HBeAg相关检测指标的明显差异,不能降低乙型肝炎表面抗原,而STSG-0002注射液给药组在给药后第一个检测时间点(给药后7天)即出现血清中HBsAg和HBeAg的显著下降,该指标在给药后14天左右达到最低值且在后续检测中维持相对稳定(中、高剂量组可降低HBsAg至基线水平且稳定维持在这一水平直至实验结束),直至最后一个检测时间点(给药后252天)未见血清中HBsAg和HBeAg显著反弹。针对给药9个月后动物解剖后的肝脏相关检测发现,STSG-0002对肝脏细胞中HBsAg和HBeAg同样表现出与血清中相关指标类似的的显著抑制效果。
小核酸基因药物STSG-0002注射液无明显全身毒性、生殖毒性、局部刺激性、免疫毒性、过敏性和溶血性风险,主要毒性靶器官为肝脏,表现为可逆性的轻微至轻度肝细胞坏死、胆管增生、炎细胞浸润。以上均属于本品的药理学作用及药理学作用的延伸相关。
STSG-0002注射液是具有自主知识产权的I类新生物制品,全新靶点,全球范围内尚无该靶点基因药物上市销售。STSG-0002注射液项目的研发成功将有效解决现有乙型肝炎患者抗病毒治疗方案不能直接降低HBsAg(乙型肝炎表面抗原)等HBV相关结构蛋白和调节蛋白的问题,有效降低HBV携带者肝脏HBV复制带来的慢性炎症,从而阻止慢性乙型肝炎患者向肝硬化、肝癌等重型肝病的进展,并将对HBV感染相关重症疾病带来新的治疗手段。
三、风险提示
本次公司获得STSG-0002注射液临床试验通知书,暂不会对公司业绩产生重大影响。本次获得新药临床试验通知书仅是新药研发进展的阶段性步骤,后续能否获得国家药品监督管理局的生产批件、获准上市尚存在诸多不确定。公司将积极推进上述研发项目,并按有关规定对该项目后续进展情况及时履行信息披露义务。
由于医药产品具有高科技、高风险、高附加值的特点,药品的前期研发以及产品从研制、临床试验报批到投产的周期长、环节多,容易受到技术、审批、政策等诸多因素影响。
特此公告
董事会
2019年09月19日

